Плюсы и минусы галогенных ламп
Спросите любого жителя мегаполиса, без чего не может обойтись современный человек. Ответы будут самыми разными, но до того момента, пока не выключат свет в квартире. Причина не важна, хоть те же самые плановые работы на подстанции. Не работает телевизор, компьютер, чайник, и в доме темно. Так что самой необходимой характеристикой оказывается именно электричество.
Важность искусственного освещения пространства даже не обсуждается. С чего же отсчитывается «лампочное летоисчисление»?
Начало всему положила обыкновенная лампа накаливания, или по-простому лампочка (кто-то кличет ее «лампой Ильича», т.к. она появилась в советскую эпоху в домах колхозников). К ней уже все привыкли, ее можно приобрести в любом магазине. Это хитрая конструкция из цоколя и специального стекла, из которой выкачали воздух. В вакууме располагается нить вольфрама. За счет электричества ниточка накаляется и дает свет, поэтому ее также называют «нитью накаливания». Огромным недостатком такого источника освещения является то, что дизайнеры не могут изменить ее форму, и им приходится под него подстраиваться.
Огромным недостатком такого источника освещения является то, что дизайнеры не могут изменить ее форму, и им приходится под него подстраиваться.
Следующим этапом эволюции этого приспособления стала лампа галогенная. При сравнении с обычным светильником она невероятное изобретение и огромный шаг вперед в оформительском и научном ключе.
Структура галогенной лампы
Светильник представляет собой что-то вроде колбы, часто двойной. Он меньше по размерам, если сравнивать его с устройством накаливания. Его колба сделана из кварца, материала, который просто не выносит никакого жира. А это значит, что при замене следует брать лампу с помощью сухой салфетки или тряпочки. В противном случае контакт с голыми руками вызовет кристаллизацию и разрушение механизма, т.е. он перегорит.
Преимущества галогенной лампы
Первое, что стоит отметить внутри нее не вакуум, а инертный газ, в который помещены галогены. Это не что иное, как бром и йод. А для чего же они применяются? Нитка вольфрама имеет свойство испаряться.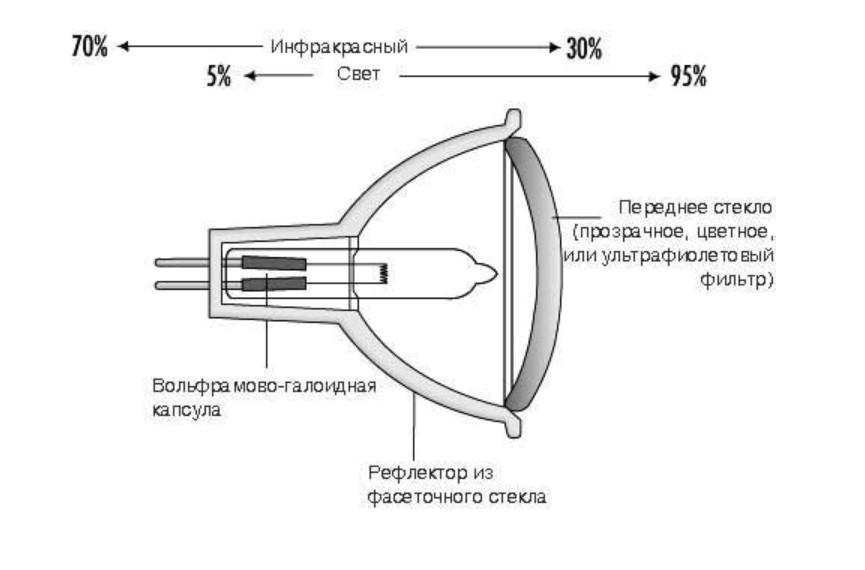 Конечно, это происходит не моментально, но довольно быстро. В среде же инертного вещества процесс замедляется, а температура накаливания сохраняется, поэтому механизм служит дольше.
Конечно, это происходит не моментально, но довольно быстро. В среде же инертного вещества процесс замедляется, а температура накаливания сохраняется, поэтому механизм служит дольше.
Второй положительный эффект от использования галогенов также важен. Как бы ни старались дизайнеры и сами обитатели помещения, от обычной лампы накаливания невозможно добиться света, полностью соответствующего задумке. Он резкий и имеет желтоватый оттенок. В галогенной лампе благодаря йоду свет получается мягким, ровным и ярким, поскольку реагент не дает стеклу вступать во взаимодействие с молекулами вольфрама, предотвращая образование легкой пленки на поверхности устройства.
Третьим плюсом галогенных световых конструкций является отношение их к классу энергосберегающих устройств.
Еще одно обстоятельство может подвигнуть вас к покупке галогенки: за счет того, что свет от нее ровный, ткани и обивка в помещении защищены от выгорания.
Минусы устройства
При покупке этого чуда техники следует знать, что одним из немногих недостатков лампочки является то, что ее колба при длительном включении сильно нагревается. Но это не должно вас настораживать. Если вместе с устройством приобрести специальный дихроичный отражатель, эта небольшая неприятность с высокой температурой его поверхности решится сама собой. В жилых пространствах самыми практичными считаются галогенные светильники с двойной колбой, оснащенные дихроичными и световыми отражателями.Небольшая рекомендация от специалистов не используйте галогенки без фильтров против ультрафиолетового излучения, которые защитят ваши глаза, кожу и предметы интерьера от вредоносного воздействия.
Но это не должно вас настораживать. Если вместе с устройством приобрести специальный дихроичный отражатель, эта небольшая неприятность с высокой температурой его поверхности решится сама собой. В жилых пространствах самыми практичными считаются галогенные светильники с двойной колбой, оснащенные дихроичными и световыми отражателями.Небольшая рекомендация от специалистов не используйте галогенки без фильтров против ультрафиолетового излучения, которые защитят ваши глаза, кожу и предметы интерьера от вредоносного воздействия.
Применение в дизайне
Именно галогенные конструкции позволят оформительской мысли без проблем решать, как подстроить освещение под свой замысел, а не отказываться от блестящих идей. Во-первых, галогенные светильники отличаются минимальными размерами, поэтому чтобы установить эти приборы не придется опускать слишком сильно потолок. Максимум на 6 см.
Во-вторых, свет можно сделать направленным, чтобы очертить определенную территорию. Сейчас стало модным зонировать пространство в комнатах. Также с помощью разноцветных защитных стекол добиться цветовой феерии в освещении стало значительно проще. А если применить еще и поверхность с рифленой структурой, свет станет «искрящимся» потоком, что выглядит невероятно эффектно, особенно в большом помещении, где нужно выделить лишь определенную часть.
Также с помощью разноцветных защитных стекол добиться цветовой феерии в освещении стало значительно проще. А если применить еще и поверхность с рифленой структурой, свет станет «искрящимся» потоком, что выглядит невероятно эффектно, особенно в большом помещении, где нужно выделить лишь определенную часть.
Виды мощности у галогенных лампочек
Эти устройства бывают разной мощности – в 220 вольт и в 12 вольт.
С первыми все довольно понятно, потому что 220 вольт это стандартное напряжение в сети. Для второго варианта вам нужно будет купить дополнительно понижающий трансформатор. При установке более чем 10 галогенных светильников, лучше взять несколько маленьких трансформаторов, чем один на всю конструкцию. Причины для этого крайне практичны.
Во-первых, чтобы заменить большой трансформатор, если он перегорит, понадобится крупное вложение средств. Во-вторых, если сломается оборудование, отвечающее за 3 светильника из 12, остальные 9 будут работать.
Галогенная лампа, конечно, имеет свои недостатки, но, по сравнению со своей предшественницей, она обладает рядом преимуществ, способных склонить рачительного хозяина и думающего дизайнера к ее использованию при оформлении пространства.
Виды галогенных ламп и их особенности
Из всех современных источников света галогенные лампы обладают наиболее качественной цветопередачей. Кроме того, галогенные лампы отличаются большой яркостью и направленным излучением. Их, конечно, только условно можно назвать энергосберегающими, тем не менее, по сравнению с лампами накаливания они имеют в несколько раз большую световую отдачу и удвоенный срок службы.
Существует очень много различных галогенных ламп. В этой статье мы познакомимся с их основными видами и особенностями.
Все галогенные лампы условно делят на две больших группы: лампы низкого напряжения (низковольтные) – до 24 В и лампы сетевого напряжение – 220 В. Кроме этого, галогенные лампы различаются по конструкции и назначению.
Основные виды галогенных ламп:
1. Линейные галогенные лампы.
Это самый старый тип галогенных ламп, которые были созданы еще в 60-х годах прошлого века.
Лампы при своих небольших размерах имеют очень приличную мощность – 1 – 20 кВт. В помещениях такие лампы не используются из-за очень высокой яркости и большой потребляемой мощности. Основная их область применения – прожекторное освещение. Существуют современные линейные галогенные лампы заливающего света, которые используют не только в наружном, но и во внутреннем освещении. Эти лампы отличаются повышенной ударопрочностью.
Линейная галогенная лампа
Лампы выпускаются стандартной длины. Наиболее популярны галогенные линейные лампы длиной 78 и 118 мм. Большинство линейных галогенных ламп требуют обязательного горизонтального размещения в пространстве. Современные линейные галогенные лампы выпускаются двухцокольными с цоколем R7s (размещен с двух сторон лампы).
2. Галогенные лампы с отражателем (галогенные лампы направленного света).
Галогенные лампы с отражателем (галогенные лампы направленного света).
Такие лампы выпускаются в стандартных типоразмерах – MR8, MR11 и MR16. Самый популярный типоразмер галогенных ламп – MR16 (диаметр колбы 50 мм). Галогенные лампы с отражателями характеризуются различными углами излучения.
Лампа состоит из миниатюрной колбы со специальным отражателем (рефлектором). Отражатели перераспределяют световой поток лампы в пространстве. Сама галогенная лампа расположена по центру отражателя.
Галогенная лампа с отражателем
Галогенные лампы с отражателем лампы обычно используют при организации точечного направленного освещения. Обычно их встраивают в подвесные и натяжные потолки, причем правильно рассчитав количество ламп, их можно применять не только в целях подсветки, но и для организации общего освещения. Такие лампы обеспечивают высокую электробезопасность. Они должны подключаются через специальный электронный или электромагнитный трансформатор.
3. Капсульные (пальчиковые) галогенные лампы.
Такие лампы имеют очень миниатюрные размеры и представляют собой небольшую капсулу с выводами. Они выпускаются с поперечными и продольными телами накала. Такие лампы могут использоваться в открытых светильниках без защитных стекол. В основном они применяются для встроенных в мебель и в потолок светильников, для декоративной подсветки. Существуют модели светильников общего освещения с капсульными галогенными лампами.
Капсульные галогенновые лампы
Возможные виды цоколей для капсульных ламп: G4, G5,3, GY6,35. Капсульные галогенные лампы сетевого напряжения обычно имеют цоколь G9 (расстояние между штырьками 9 мм). Они используются для декоративной подсветки, и иногда в светильниках для общего освещения.
В этой статье описаны только основные виды галогенных ламп. Безусловно, производители источников света не стоят на месте и каждый год совершенствуют выпускаемые галогенные лампы, а также создают их новые разновидности, что и подтверждается постоянным обновлением нашего ассортимента в каталогах!
Безусловно, производители источников света не стоят на месте и каждый год совершенствуют выпускаемые галогенные лампы, а также создают их новые разновидности, что и подтверждается постоянным обновлением нашего ассортимента в каталогах!
Преимущества галогенной лампы TM Econ:
- Высокая степень световой отдачи;
- Срок службы в 2 раза превышает показатели обычной лампы;
- Значительная экономия электроэнергии;
- Производят яркий и ровный свет, без нагрузки на глаза.
Галоген | Элементы, примеры, свойства, использование и факты
Таблица Менделеева
Просмотреть все СМИ
- Ключевые люди:
- Жан-Батист-Андре Дюма
- Похожие темы:
- галогенорганическое соединение йод фтор хлор бром
Просмотреть весь связанный контент →
Популярные вопросы
Что такое галогенные элементы?
Галогенные элементы представляют собой шесть элементов 17-й группы периодической таблицы. Группа 17 занимает вторую колонку справа в периодической таблице и содержит фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Астат и теннессин являются радиоактивными элементами с очень коротким периодом полураспада и поэтому не встречаются в природе.
Группа 17 занимает вторую колонку справа в периодической таблице и содержит фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Астат и теннессин являются радиоактивными элементами с очень коротким периодом полураспада и поэтому не встречаются в природе.
Каковы основные свойства галогенных элементов?
Галогенные элементы очень реакционноспособны. С натрием они производят соли, из которых наиболее известна поваренная соль (хлорид натрия, NaCl). Каждый атом галогена имеет семь валентных электронов на внешней электронной оболочке. Поэтому, когда атом галогена может получить электрон от атома другого элемента, два атома образуют очень стабильное соединение, потому что тогда самая внешняя электронная оболочка атома галогена заполнена.
В каких случаях используются галогеновые элементы?
Хлор используется для очистки воды. Кроме того, хлор входит в состав поваренной соли, хлорида натрия, который является одним из наиболее широко используемых химических соединений. Фтор используется во фторидах, которые добавляют в воду для предотвращения кариеса. Йод используется как антисептик.
Фтор используется во фторидах, которые добавляют в воду для предотвращения кариеса. Йод используется как антисептик.
Почему эти элементы называются галогенами?
При взаимодействии этих элементов с натрием образуются соли. Наиболее известным из них является хлорид натрия или обычная поваренная соль (также называемая галитом). Слово галоген происходит от греческих корней hal-, что означает «соль», и -gen , что означает «производить».
Сводка
Прочтите краткий обзор этой темы
галоген , любой из шести неметаллических элементов, составляющих группу 17 (группа VIIa) периодической таблицы. Галогенсодержащие элементы: фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Им дали название галоген 9.0046 , от греческих корней hal — («соль») и — gen («производить»), потому что все они производят натриевые соли со схожими свойствами, из которых лучше всего подходит хлорид натрия — поваренная соль, или галит. известен.
известен.
Свободные галогены не встречаются в природе из-за их большой реакционной способности. В комбинированной форме фтор является самым распространенным из галогенов в земной коре. Процентное содержание галогенов в изверженных породах земной коры: фтора 0,06, хлора 0,031, брома 0,00016, йода 0,00003. Астатин и теннессин не встречаются в природе, так как состоят только из короткоживущих радиоактивных изотопов.
Галогенные элементы имеют большое сходство друг с другом в их общем химическом поведении и в свойствах их соединений с другими элементами. Однако наблюдается прогрессивное изменение свойств от фтора через хлор, бром и йод к астату — разница между двумя последовательными элементами наиболее заметна для фтора и хлора. Фтор является наиболее реакционноспособным из галогенов и, фактически, из всех элементов, и у него есть некоторые другие свойства, которые отличают его от других галогенов.
Хлор является наиболее известным из галогенных элементов. Свободный элемент широко используется в качестве реагента для очистки воды и используется в ряде химических процессов. Поваренная соль, хлорид натрия, безусловно, является одним из самых привычных химических соединений. Фториды известны главным образом тем, что их добавляют в воду для предотвращения кариеса, но органические фториды также используются в качестве хладагентов и смазочных материалов. Йод наиболее известен как антисептик, а бром используется в основном для получения соединений брома, которые используются в антипиренах и в качестве пестицидов общего назначения. В прошлом дибромид этилена широко использовался в качестве присадки к этилированному бензину.
Поваренная соль, хлорид натрия, безусловно, является одним из самых привычных химических соединений. Фториды известны главным образом тем, что их добавляют в воду для предотвращения кариеса, но органические фториды также используются в качестве хладагентов и смазочных материалов. Йод наиболее известен как антисептик, а бром используется в основном для получения соединений брома, которые используются в антипиренах и в качестве пестицидов общего назначения. В прошлом дибромид этилена широко использовался в качестве присадки к этилированному бензину.
Britannica Quiz
Периодическая таблица элементов
Вероятно, самое важное обобщение, которое можно сделать о галогенных элементах, состоит в том, что все они являются окислителями; то есть они повышают степень окисления или степень окисления других элементов — свойство, которое раньше приравнивалось к соединению с кислородом, но теперь интерпретируется в терминах переноса электронов от одного атома к другому. При окислении другого элемента восстанавливается сам галоген; т. е. степень окисления 0 свободного элемента снижается до -1. Галогены могут соединяться с другими элементами, образуя соединения, известные как галогениды, а именно фториды, хлориды, бромиды, йодиды и астатиды. Многие из галогенидов можно рассматривать как соли соответствующих галогеноводородов, которые при комнатной температуре и атмосферном давлении представляют собой бесцветные газы и (за исключением фтороводорода) образуют в водном растворе сильные кислоты. Действительно, общий термин 9Соль 0045
При окислении другого элемента восстанавливается сам галоген; т. е. степень окисления 0 свободного элемента снижается до -1. Галогены могут соединяться с другими элементами, образуя соединения, известные как галогениды, а именно фториды, хлориды, бромиды, йодиды и астатиды. Многие из галогенидов можно рассматривать как соли соответствующих галогеноводородов, которые при комнатной температуре и атмосферном давлении представляют собой бесцветные газы и (за исключением фтороводорода) образуют в водном растворе сильные кислоты. Действительно, общий термин 9Соль 0045
Окислительная сила галогенов возрастает в том же порядке, т. е. от астата к фтору. Поэтому из галогенных элементов с наибольшим трудом получается элементарный фтор, с наименьшим — йод. Галогенные элементы как класс относятся к неметаллам, но астат проявляет определенные свойства, напоминающие свойства металлов.
е. от астата к фтору. Поэтому из галогенных элементов с наибольшим трудом получается элементарный фтор, с наименьшим — йод. Галогенные элементы как класс относятся к неметаллам, но астат проявляет определенные свойства, напоминающие свойства металлов.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Химическое поведение галогенных элементов удобнее всего обсуждать с точки зрения их положения в периодической таблице элементов. В периодической таблице галогены составляют группу 17 (согласно системе нумерации, принятой Международным союзом теоретической и прикладной химии), группу, непосредственно предшествующую благородным газам. Атомы галогенов несут семь валентных электронов на внешней электронной оболочке. Эти семь крайних электронов находятся на двух различных орбиталях, обозначенных как 9.0045 s (с двумя электронами) и p (с пятью). Потенциально атом галогена может содержать еще один электрон (на орбитали p ), что придаст образующемуся иону галогенида такое же расположение (конфигурацию), что и благородный газ рядом с ним в периодической таблице. Эти электронные конфигурации исключительно стабильны. Эта ярко выраженная склонность галогенов приобретать дополнительный электрон делает их сильными окислителями.
Эти электронные конфигурации исключительно стабильны. Эта ярко выраженная склонность галогенов приобретать дополнительный электрон делает их сильными окислителями.
При комнатной температуре и атмосферном давлении галогенные элементы в свободном состоянии существуют в виде двухатомных молекул. В молекулярном фторе (F 2 ) атомы удерживаются вместе связью, состоящей из объединения p орбиталей каждого атома, при этом такая связь классифицируется как сигма-связь. Следует отметить, что энергия диссоциации фтора (энергия, необходимая для разрыва связи F—F) более чем на 30 % меньше, чем у хлора, но аналогична энергии йода (I 2 ). Слабость одинарной связи F—F по сравнению с хлором можно объяснить небольшим размером фтора, что приводит к уменьшению перекрывания связывающих орбиталей и увеличению отталкивания несвязывающих орбиталей. Однако в йоде p орбитали более размыты, что означает, что связь становится слабее, чем в хлоре или броме.
Британика
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- В этот день в истории
- Викторины
- Подкасты
- Словарь
- Биографии
- Резюме
- Популярные вопросы
- Обзор за неделю
- Инфографика
- Демистификация
- Списки
- #WTFact
- Товарищи
- Галереи изображений
- Прожектор
- Форум
- Один хороший факт
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- Britannica объясняет
В этих видеороликах Britannica объясняет различные темы и отвечает на часто задаваемые вопросы.
- Britannica Classics
Посмотрите эти ретро-видео из архивов Encyclopedia Britannica. - #WTFact Видео
В #WTFact Britannica делится некоторыми из самых странных фактов, которые мы можем найти. - На этот раз в истории
В этих видеороликах узнайте, что произошло в этом месяце (или любом другом месяце!) в истории. - Demystified Videos
В Demystified у Britannica есть все ответы на ваши животрепещущие вопросы.
- Студенческий портал
Britannica — это главный ресурс для учащихся по ключевым школьным предметам, таким как история, государственное управление, литература и т. д. - Портал COVID-19
Хотя этот глобальный кризис в области здравоохранения продолжает развиваться, может быть полезно обратиться к прошлым пандемиям, чтобы лучше понять, как реагировать сегодня. - 100 женщин
Britannica празднует столетие Девятнадцатой поправки, выделяя суфражисток и политиков, творящих историю.


